▶ 6월 미국 FDA 신약 승인 동향은 대체로 부진. 가장 기대했던 글로벌 블록버스터 최초 NASH 치료제 오칼리바는 보완요구공문(CRL) 받았음. 새로운 혁신 신약 승인은 지연되고 있는 가운데, 기존 글로벌 메가 블록버스터 면역항암제 키트루다는 3개 적응증 추가되며, ‘23년 가장 잘 팔리는 의약품이 될 것으로 전망됨.
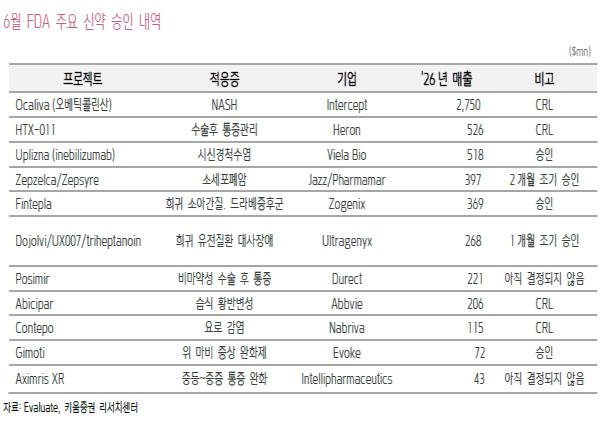 |
◎ 글로벌 블록버스터 NASH 신약 오칼리바 CRL 받는 등 신약 승인 부재
>> 6월, 4개 제품이 최종보완요구공문(CRL) 받았는데, 가장 눈에 띄는 것은 ‘26년 $2.6bn의 글로벌 블록버스터 신약을 예상했던 Intercept의 비알코올성지방간염(NASH) 치료제 오베틱콜릭산(obeticholic acid) 이었으며 이로 인해 Intercept 주가 40% 하락. 오베티콜릭산은 혁신치료제로 지정된 유일한 NASH 치료제 후보물질임.
>> Keytruda는 3가지 추가 적응증 승인 받았음. Evaluate은 ‘23년 가장 잘 팔리는 의약품이 될 것으로 예상되고 있으며, ‘26년 $25bn 매출 예상됨.
ᆞ키트루다, 단일요법으로 전이성 MSI-H/dMMR 대장암 1차 치료 승인.
ᆞ메드팩토, 키트루다와 대장암 국내 1/2상 중. (MSS, MSI-H 구분 없는 병용 1/2상 ORR 33.3%, 키트루다 0% *직접 비교아님)
>> 코로나19 치료제에 많은 인력 투여와 자원 집중되고 있는 가운데 주요 혁신 신약 승인 또한 지연되고 있음.
ᆞ6/30일까지 25개 제품 FDA 승인됨
ᆞ노바티스의 다발성결화증 치료제 ofatumumab SC제형 승인 결정 9월로 지연되었으며, 특별한 사유 밝히지 않았음.
ᆞGSK의 다발성골수종 BCMA-ADC 치료제 belantamab mafodotin 미팅 7/14일로 연기됨.
ᆞ올해 미국 신약 승인 앞둔 제품은 한미약품/스펙트럼의 호중구감소증 치료제 롤론티스 BLA 검토 기한은 PDUFA(전문의약품 허가 신청자 비용 부담법)에 따라 10/24일까지임. <자료제공:키움증권>
 |
박병우 기자 bwpark0918@pharmstock.co.kr






