- 알츠하이며 치료제 선급금 1200억...올해 임상 3상 정점 돌입
 |
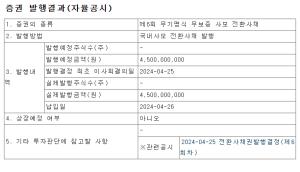
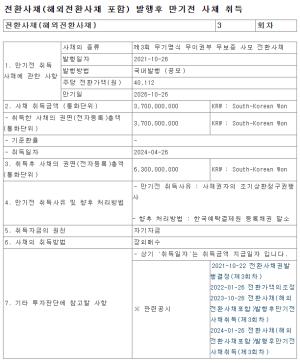
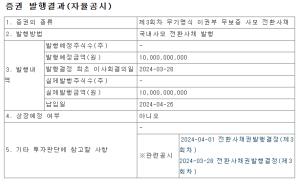
아리바이오는 중국 제약사와 7억7000만 달러(약 1조200억원) 규모의 경구용 치매치료제 'AR1001' 중국 독점 판권 계약을 체결했다고 25일 밝혔다.
올해 중반기부터 선급금 1200억원을 일정에 따라 받는 조건이다. 이후 임상 개발·허가 단계별 기술료(Milestone)와 판매에 따른 로열티 9000억원을 받는다.
계약금은 반환 조건이 없다. 아리바이오는 복수의 글로벌 국가들과 판권 계약 협상을 진행 중이며, 치매 신약에 대한 중국 내 경쟁 상황과 판매전략을 고려해 중국 측 기업의 요청으로 계약사는 추후 공개할 계획이라고 밝혔다. 아리바이오는 AR1001에 대해 국내에서는 삼진제약과도 1000억원 규모의 독점 판매계약을 맺었다.
AR1001은 PDE5 억제제로, 알츠하이머병의 복잡하고 다양한 병리를 동시에 공략할 수 있는 다중기전 경구용 치료제로 개발되고 있다. 2021년 12월 미국 클리블랜드 대학 연구팀이 PDE5 억제제 계열의 약물이 알츠하이머병을 69% 예방한다는 연구결과를 발표했고, 올해 2월 영국 유니버시티 칼리지 런던의 연구팀도 유사한 결과를 발표한 바 있다.
논문 및 글로벌 학회 발표 등으로 AR1001의 다중기전으로 뇌 신경세포 사멸 억제 및 생성 촉진, 뇌 신호 전달체계 활성화와 시냅스 가소성 증진, 독성 단백질 제거 및 우수한 뇌 장벽 투과성 등이 확인됐다. 알츠하이머병의 주요 바이오마커인 타우 및 GFAP (염증 관련 마커) 개선도 세포와 동물 실험 및 임상 시험에서 나타났다.
AR1001의 신약 허가용 글로벌 임상 3상(Polaris AD)은 현재 약 1150명 규모로 진행중이다. 2022년 12월 미국 (FDA)에서 첫 환자 투약이 시작돼 미 전역 70여개 임상센터에서 환자 모집과 투약이 진행중이다. 한국 (MFDS)은 임상3상 허가를 받고 2월부터 환자 모집과 투약이 진행되고 있다. 영국은 최근 임상3상 시험 허가를 받았다.
정재준 아리바이오 대표는 "올해 글로벌 임상3상이 정점에 돌입하고, 미충족 수요가 큰 치매치료제의 시급성과 중요성을 살펴 최종 임상 성공과 신약 허가, 출시까지 박차를 가할 것"이라고 말했다.
박병우 기자 bwpark0918@pharmstock.co.kr